Ртуть
РТУТЬ -и; ж. Химический элемент (Hg), жидкий тяжёлый металл серебристо-белого цвета (широко применяется в химии и электротехнике). Живой, как ртуть. (очень подвижный).
◊ Гремучая ртуть Взрывчатое вещество в виде белого или серого порошка.
ртуть(лат. Hydrargyrum), химический элемент II группы периодической системы. Серебристый жидкий металл (отсюда латинское название; от греческого hýdōr - вода и árgyros - серебро). Плотность при 20°C 13,546 г/см 3 (тяжелее всех известных жидкостей), t пл –38,87°C, t кип 356,58°C. Пары ртути при высокой температуре и при электрическом разряде излучают голубовато-зелёный свет, богатый ультрафиолетовыми лучами. Химически стойка. Основной минерал - киноварь HgS; встречается также ртуть самородная. Используется при изготовлении термометров, манометров, газоразрядных приборов, в производстве хлора и гидроксида натрия (как катод). Сплавы ртути с металлами - амальгамы. Ртуть и многие её соединения ядовиты.
РТУТЬРТУ́ТЬ (лат. Hydrargyrum), Hg (читается «гидраргирум»), химический элемент с атомным номером 80, атомная масса 200,59.
Природная ртуть состоит из смеси семи стабильных нуклидов: 196 Hg (содержание 0,146% по массе), 198 Hg (10,02%), 199 Hg (16,84%), 200 Hg (23,13%), 201 Hg (13,22%), 202 Hg (29,80%) и 204 Hg (6,85%). Радиус атома ртути 0,155 нм. Радиус иона Hg + - 0,111 нм (координационное число 3), 0,133 нм (координационное число 6), иона Hg 2+ - 0,083 нм (координационное число 2), 0,110 нм (координационное число 4), 0,116 нм (координационное число 6) или 0,128 нм (координационное число 8). Энергии последовательной ионизации нейтрального атома ртути равны 10,438, 18,756 и 34,2 эВ.
Расположена во IIВ группе, 6 периода периодической системы. Конфигурация внешнего и предвнешнего электронных слоев 5s
2
p
6
d
10
6s
2
. В соединениях проявляет степени окисления +1 и +2. Электроотрицательность по Полингу (см.
ПОЛИНГ Лайнус)
1,9.
История открытия
Ртуть известна человечеству с древнейших времен. Обжиг киновари (см.
КИНОВАРЬ)
HgS, приводящий к получению жидкой ртути, использовали еще в 5 в. до н. э. в Междуречье (см.
МЕСОПОТАМИЯ)
. Использование киновари и жидкой ртути описано в древних документах Китая, Ближнего Востока. Первое подробное описание получения ртути из киновари описано Теофрастом (см.
ТЕОФРАСТ)
около 300 лет до н. э.
В древности ртуть использовали для добычи золота (см.
ЗОЛОТО (химический элемент))
из золотых руд. Этот способ основан на ее способности растворять многие металлы, образуя жидкие или легкоплавкие амальгамы (см.
АМАЛЬГАМА)
. При прокаливании амальгамы золота летучая ртуть испаряется, золото остается. Во второй половине 15 в в Мексике применяли амальгамирование для извлечения из руды серебра (см.
СЕРЕБРО)
.
Алхимики считали ртуть составной частью всех металлов, полагая, что изменением ее содержания можно осуществить превращение ртути в золото. Только в 20 в. физики установили, что в процессе ядерной реакции атомы ртути действительно превращаются в атомы золота. Но такой способ чрезвычайно дорог.
Жидкая ртуть - очень подвижная жидкость. Алхимики называли ртуть «меркурием» по имени римского бога Меркурия, славившегося своей быстротой в перемещении. В английском, французском, испанском и итальянском языках для ртути используется название «mercury». Современное латинское название происходит от греческих слов «хюдор» - вода и «аргирос» - серебро, т. е. «жидкое серебро».
Ртутные препараты использовали в медицине в средние века (ятрохимия (см.
ЯТРОХИМИЯ)
).
Нахождение в природе
Редкий рассеянный элемент. Содержание ртути в земной коре 7,0·10 –6 % по массе. В природе ртуть встречается в свободном состоянии. Образует более 30 минералов. Основной рудный минерал киноварь. Минералы ртути в виде изоморфных примесей встречаются в кварце, халцедоне, карбонатах, слюдах, свинцово-цинковых рудах. Желтая модификация HgO встречается в природе в виде минерала монтроидита. В обменных процессах литосферы, гидросферы, атмосферы участвует большое количество ртути. Содержание ртути в рудах от 0,05 до 6-7%.
Получение
Первоначально ртуть получали из киновари (см.
КИНОВАРЬ)
, помещая ее куски в вязанки хвороста и обжигая киноварь в кострах.
В настоящее время ртуть получают окислительно-восстановительным обжигом руд или концентратов при 700-800 о С в печах кипящего слоя, трубчатых или муфельных. Условно процесс может быть выражен:
HgS + O 2 = Hg + SO 2
Выход ртути при таком способе составляет около 80%. Более эффективен способ получения ртути путем нагревания руды с Fe (см.
ЖЕЛЕЗО)
и CaO:
HgS + Fe = Hg – + FeS,
4HgS + 4CaO = 4Hg – + 3CaS + CaSO 4 .
Особо чистую ртуть получают электрохимическим рафинированием на ртутном электроде. При этом содержание примесей составляет от 1·10 –6 до 1·10 –7 %.
Физические и химические свойства
Ртуть - серебристо-белый металл, в парах бесцветный. Единственный жидкий при комнатной температуре металл. Температура плавления –38,87°C, кипения 356,58°C. Плотность жидкой ртути при 20°C 13,5457 г/см 3 , твердой ртути при –38,9°C - 14,193 г/см 3 .
Твердая ртуть - бесцветные кристаллы октаэдрической формы, существующая в двух кристаллических модификациях. «Высокотемпературная» модификация обладает ромбоэдрической решеткой a-Hg, параметры ее элементарной ячейки (при 78 К) а= 0,29925 нм, угол b = 70,74 о. Низкотемпературная модификация b-Hg обладает тетрагональной решеткой (ниже 79К).
С использованием ртути голландский физик и химик Х.Камерлинг-Оннес (см.
КАМЕРЛИНГ-ОННЕС Хейке)
в 1911 впервые наблюдал явление сверхпроводимости (см.
СВЕРХПРОВОДИМОСТЬ)
. Температура перехода a-Hg в сверхпроводящее состояние 4,153К, b-Hg - 3,949К. При более высоких температурах ртуть ведет себя как диамагнетик (см.
ДИАМАГНЕТИК)
. Жидкая ртуть не смачивает стекло и практически не растворяется в воде (в 100 г воды при 25°C растворяется 6·10 –6 г ртути).
Стандартный электродный потенциал пары Hg 2+ 2 /Hg 0 = +0.789 B, пары Hg 2+ /Hg 0 = +0.854B, пары Hg 2+ /Hg 2+ 2 = +0.920B. В неокисляющих кислотах ртуть не растворяется с выделением водорода (см.
ВОДОРОД)
. (см.
КИСЛОРОД)
Кислород (см.
КИСЛОРОД)
и сухой воздух при обычных условиях ртуть не окисляют. Влажный воздух и кислород при ультрафиолетовом облучении или электронной бомбардировке окисляют ртуть с поверхности с образованием оксидов.
Ртуть окисляется кислородом воздуха при температуре выше 300°C, образуя оксид ртути HgO красного цвета:
2Hg + O 2 = 2HgO.
Выше 340°C этот оксид разлагается на простые вещества.
При комнатной температуре ртуть окисляется озоном (см.
ОЗОН)
.
Ртуть не реагирует при нормальных условиях с молекулярным водородом, но с атомарным водородом образует газообразный гидрид HgH. Ртуть не взаимодействует с азотом, фосфором, мышьяком, углеродом, кремнием, бором, германием.
С разбавленными кислотами ртуть не реагирует, но растворяется в царской водке (см.
ЦАРСКАЯ ВОДКА)
и в азотной кислоте. Причем, в случае с кислотой продукт реакции зависит от концентрации кислоты и соотношения ртути и кислоты. При избытке ртути, на холоду, протекает реакция:
6Hg + 8HNO 3 разбавл. = 3Hg 2 (NO 3) 2 + 2NO + 4H 2 O.
При избытке кислоты:
3Hg + 8HNO 3 = 3Hg(NO 3) 2 + 2NO + 4H 2 O.
С галогенами (см.
ГАЛОГЕНЫ)
ртуть активно взаимодействует с образованием галогенидов (см.
ГАЛОГЕНИДЫ)
. При реакциях ртути с серой (см.
СЕРА)
,
селеном (см.
СЕЛЕН)
и теллуром (см.
ТЕЛЛУР)
возникают халькогениды (см.
ХАЛЬКОГЕНИДЫ)
HgS, HgSe, HgTe. Эти халькогениды праrтически не растворимы в воде. Например, значение ПР HgS = 2·10 –52 . Сульфид ртути растворяется только в кипящей HCl, царской водке (при этом образуется комплекс 2–) и в концентрированных растворах сульфидов щелочных металлов:
HgS + K 2 S = K 2 .
Сплавы ртути с металлами называют амальгамами (см.
АМАЛЬГАМА)
. Стойкие к амальгамированию металлы - железо (см.
ЖЕЛЕЗО)
,
ванадий (см.
ВАНАДИЙ)
,
молибден (см.
МОЛИБДЕН)
,
вольфрам (см.
ВОЛЬФРАМ)
,
ниобий (см.
НИОБИЙ)
и тантал (см.
ТАНТАЛ (химический элемент))
. Со многими металлами ртуть образует интерметаллические соединения меркуриды.
Ртуть образует два оксида: оксид ртути(II) HgO и неустойчивый на свету и при нагревании оксид ртути(I) Hg 2 O (черные кристаллы).
HgO образует две модификации - желтую и красную, отличающиеся размерами кристаллов. Красная модификация образуется при добавлении к раствору соли Hg 2+ щелочи:
Hg(NO 3) 2 + 2NaOH = HgOЇ + 2NaNO 3 + H 2 O.
Желтая форма химически более активна, при нагревании краснеет. Красная форма при нагревании чернеет, но приобретает прежний цвет при охлаждении.
При добавлении щелочи к раствору соли ртути(I) образуется оксид ртути (I) Hg 2 O:
Hg 2 (NO 3) 2 + 2NaOH = Hg 2 O + H 2 O + 2NaNO 3 .
На свету Hg 2 O распадается на ртуть и HgO, давая осадок черного цвета.
Для соединений ртути(II) характерно образование устойчивых комплексных соединений (см.
КОМПЛЕКСНЫЕ СОЕДИНЕНИЯ)
:
2KI + HgI 2 = K 2 ,
2KCN + Hg(CN) 2 = K 2 .
Соли ртути(I) содержат группировку Hg 2 2+ со связью –Hg–Hg–. Получают эти соединения, восстанавливая соли ртути(II) ртутью:
HgSO 4 + Hg + 2NaCl = Hg 2 Cl 2 + Na 2 SO 4 ,
HgCl 2 + Hg = Hg 2 Cl 2 .
В зависимости от условий, соединения ртути(I) могут проявлять как окислительные, так и восстановительные свойства:
Hg 2 Cl 2 + Cl 2 = 2HgCl 2 ,
Hg 2 Cl 2 + SnCl 2 = 2Hg + SnCl 4 . (см.
ПЕРОКСИДНЫЕ СОЕДИНЕНИЯ)
Пероксид (см.
ПЕРОКСИДНЫЕ СОЕДИНЕНИЯ)
HgO 2 - кристаллы; неустойчив, взрывается при нагревании и ударе.
Применение
Ртуть используют для изготовления катодов при электрохимическом получении едких щелочей и хлора, а также для полярографов, в диффузионных насосах, барометрах и манометрах; для определения чистоты фтора и его концентрации в газах. Парами ртути наполняют колбы газоразрядных ламп (ртутных и люминесцентных) и источников УФ излучения. Ртуть применяют при нанесении золотых покрытий и при добычи золота из руды. (см.
)
Сулема (см.
)
- важнейший антисептик, применяют при разбавлениях 1:1000. Оксид ртути (II), киноварь HgS применяются для лечения глазных и кожных и венерических заболеваний. Киноварь также используют для приготовления чернил и красок. В древности из киновари готовили румяна. Каломель (см.
КАЛОМЕЛЬ)
используется в ветеринарии в качестве слабительного средства.
Физиологическое действие
Ртуть и ее соединения высокотоксичны. Пары и соединения ртути накапливаясь в организме человека, сорбируются легкими, попадают в кровь, нарушают обмен веществ и поражают нервную систему. Признаки ртутного отравления проявляются уже при содержании ртути в концентрации 0.0002–0.0003 мг/л. Пары ртути фитотоксичны, ускоряют старение растений.
При работе с ртутью и ее соединениями следует предотвращать ее попадание в организм через дыхательные пути и кожу. Хранят в закрытых сосудах.
Энциклопедический словарь . 2009 .
Синонимы :Смотреть что такое "ртуть" в других словарях:
Ртуть, и … Русский орфографический словарь
Ртуть/ … Морфемно-орфографический словарь
РТУТЬ, Hydrargyrum (от греч. hydor вода и argyros серебро), Mercurium, Hydrargyrum VІvum, s. metallicum, Mercurius VІvus, Argentum VІvum, серебристо белый жидкий металл, симв. Hg, ат. в. 200,61; уд. в. 13,573; ат. объем 15,4; t° замерз.… … Большая медицинская энциклопедия
Ртуть – это единственный из известных человеку металлов, который остается жидким при комнатной температуре. Внешне ртуть напоминает жидкое серебро; при попадании на плоскую поверхность капля ртути моментально рассыпается на сотни мельчайших шариков, которые словно отталкиваются друг от друга и разбегаются в разные стороны.
Ртуть – очень редкий элемент. В целом в природе ртуть образуется в процессе окисления киновари и разложения образующегося сульфата; во время ; путем выделения из водных растворов. В земной коре ртуть рассеяна, а в результате осаждения из горячих подземных вод она образует ртутные руды.
На сегодняшний день известно 35 ртутьсодержащих минералов. Некоторое количество ртути содержится в морской воде, в сланцах и глинах.
Из истории вопроса
Уже за две тысячи лет до нашей эры в Древней Индии и Древнем Китае умели добывать самородную ртуть. Ртуть, содержащую киноварь уже тогда использовали в лечении и косметологии. В ходе экспериментов древних ученых нагретая киноварь оседала на металле в виде «жидкого серебра».
Алхимики уделяли ртути огромное значение – считалось, что после того, как ртуть затвердевает, она может превращаться в золото. Впервые твердую ртуть удалось получить Ломоносову – он использовал для этого смесь снега и концентрированной азотной кислоты.
Где используют ртуть?
Ртуть незаменима при изготовлении различных метрологических приборов – , термометров, полярографов, вакуумных насосов. Ртуть является важным элементом при производстве ртутных ламп, выпрямителей. Кроме того, этот металл активно применяют в химической промышленности и металлургии.
Ртуть – катализатор при различных реакциях, важный элемент при амальгамации других металлов. Ее применяют в медицине, промышленности и сельском хозяйстве. Именно ртутное покрытие позволяет выпускать зеркала, без которых нам не обойтись.
Основные свойства ртути
Это серебристый, тяжелый, жидкий металл, который при комнатной температуре испаряется. Чем выше температура воздуха, тем быстрее происходит испарение. Ртуть (химическая формула Hg) взаимодействует с серебром, золотом, цинком, смачивая их и образуя амальгамы. Ртуть кипит при температуре +357.25 С.
По степени опасности относится к первому классу и является чрезвычайно мощным загрязнителем окружающей среды – воздуха, почвы, воды. Ртуть и ее соединения крайне токсичны и опасны для организма человека.
Опасность ртути
Попадая в организм через легкие, пары ртути вызывают острые и хронические отравления. Ртуть поражает органы дыхания, печень, центральную нервную систему, желудочно-кишечный тракт, сердечно-сосудистую систему, прочие внутренние органы. Симптомы токсичного поражения проявляются через 8-24 часа.
У пострадавшего наблюдается слабость, апатия, эмоциональная неустойчивость, головокружение, головная боль. Ослабляется внимание и память, появляется потливость, боли при глотании, повышается температура, начинаются боли в желудке, тошнота, рвота, повышается температура, появляется тремор рук.
При серьезном отравлении не исключен летальный исход. В организм ртуть проникает чаще всего через легкие – человек вдыхает опасные пары, которые не имеют запаха.
Меры предосторожности и способы хранения
При работе с ртутью нужно использовать противогазы или фильтрующие респираторы. Если произошло ртутное загрязнение, проводятся меры по демеркуризации. Видимые количества металлической ртути устраняют с загрязненных поверхностей, после этого осуществляют химическую обработку при помощи химических реагентов.
Ртуть, которую используют в промышленности, хранят в стальных баллонах емкостью не более 35 кг, в керамических или стеклянных баллонах емкостью 500 мл с толстыми стенами, металлической гофрированной пробкой с прокладкой из пластмассы. В каждом баллоне помещается 5 кг ртути.
В лабораториях ртуть хранят в запаянных стеклянных ампулах по 30-40 мл в каждой, которые, опускают в сварные стальные коробки. Ртуть нельзя хранить в открытой посуде, а также в бюксах, колбах и прочей химической посуде с тонкими стенками.
Ртуть – один из редких элементов Земной коры, выглядит как блестящий серебристо-белый тяжёлый металл. В обычных условиях он остаётся жидким и необычайно подвижным. Твёрдым металлом ртуть может стать при -39° С. При комнатной температуре легко испаряется, не имея запаха и вкуса, чем представляет угрозу отравления. В быту источником отравления может служить разбитый градусник.
Чистый металл ртути получают из минеральной руды, называемой киноварь, которую разогревают до высоких температур, ртуть выпаривается и конденсируется.
Где находит применение ртуть
Уникальные свойства сделали ртуть в современных отраслях промышленности важным элементом. Нет такой отрасли, где бы не использовался этот необычный металл:
Ртуть – вещество, при утечке которого человек должен действовать молниеносно. При правильном устранении последствий появляется возможность оперативно оградить себя от вредных паров ртути. А вовремя оказанная помощь способна спасти жизнь человеку.
В сравнении с лампами накаливания современные энергосберегающие лампы обладают очевидными достоинствами. Но из-за особенностей конструкции пользоваться ими нужно осторожно и принять меры, если разбилась энергосберегающая лампочка.
Сегодня хорошо известно какое негативное воздействие на здоровье оказывает ртуть, поэтому важно уметь правильно утилизовать разбившийся ртутный градусник
В целях экономии энергетических ресурсов, все чаще применяются лампы дневного света, но в конструкции этих световых приборов используется ртуть, опасный металл, который должен подлежать обязательной утилизации
Как ртуть действует в приборах
Электрический аккумулятор
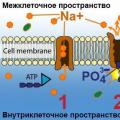
Содержит диоксисульфатно-ртутный элемент. Который является химическим источником тока. Электролитом выступает водный раствор сульфата цинка, анодом – цинк, катодом – смесь графита с окисью ртути и сульфатом ртути.
Типы таких аккумуляторов используются в мобильных телефонах, ноутбуках, цифровых фотоаппаратах.
 Устройство, позволяющее проводить электрохимический анализ веществ и химических процессов. В исследуемый раствор погружают один поляризующийся капельно-ртутный электрод, другой – неполяризующийся электрод с большой поверхностью, покрытой слоем ртути. Затем на электроды поступает возрастающее напряжению. Величина тока, проходимого через раствор, измеряется гальванометром. На основании полученных замеров строят полярограмму.
Устройство, позволяющее проводить электрохимический анализ веществ и химических процессов. В исследуемый раствор погружают один поляризующийся капельно-ртутный электрод, другой – неполяризующийся электрод с большой поверхностью, покрытой слоем ртути. Затем на электроды поступает возрастающее напряжению. Величина тока, проходимого через раствор, измеряется гальванометром. На основании полученных замеров строят полярограмму.
Методом полярографии проводят исследования состава вредных веществ в промышленных выбросах, определяют степень насыщенности крови кислородом, диагностируют такие заболевания как злокачественные опухоли, лучевую болезнь полярограммой сыворотки крови.
Люминесцентные и кварцевые лампы
Конструкция состоит из герметической колбы (стеклянной либо кварцевой), наполненной смесью газов и паров ртути, и прикреплённых с двух сторон электродов. Через контакты подаётся электрический разряд и в колбе возникают невидимые ультрафиолетовые лучи, для трансформации которых в видимый свет поверхность колбы изнутри покрыта слоем люминофора. Различный состав покрытия можно получить разнообразную цветовую гамму. Ультрафиолетовое излучение имеет бактерицидное действие, медицина использует это свойство в профилактических и противоэпидемиологических целях.
Барометр
Внутри прибора размещена запаянная с одной стороны колба с ртутью, реагирующая на малейшие перепады атмосферного давления. В зависимости от происходящих изменений столбик ртути, поднимаясь или опускаясь по шкале барометра, показывает предполагаемую погоду.

Используется для измерения кровяного давления человека.
По принципу сообщающихся сосудов ртуть, находящаяся в стеклянной трубке, поднимается в результате подачи сдавленного с помощью резиновой груши воздуха.
По шкале трубки производится отсчёт давления.
Отличается высокой точностью по сравнению с новоявленными приборами на , но промышленностью уже не выпускается.
Термометры
Основаны на свойстве ртути менять свой объём под воздействием температуры. Состоит из стеклянного резервуара, наполненного ртутью, и шкалы, цена деления которой имеет широкий диапазон в зависимости от назначения термометра (от -39°С до +357°С).
Ртутный диффузионный насос
Входит в сборку вакуумных установок и с его помощью достигается глубокий вакуум. Служит для откачки газа или пара из рабочей камеры насоса. Процесс происходит в результате периодического изменения давления внутри камеры посредством нагрева и последующего охлаждения ртути. Газ стремится в область с пониженным давлением, создавая вакуум.
Ртуть опасна для здоровья
 Восьмидесятый элемент таблицы Менделеева признан глобальным загрязнителем окружающей среды. По нанесению вреда жизни и здоровью людей он относится к первому классу опасности. Поставщиками ртути в атмосферу являются предприятия и заводы
, использующие её в своём производстве.
Восьмидесятый элемент таблицы Менделеева признан глобальным загрязнителем окружающей среды. По нанесению вреда жизни и здоровью людей он относится к первому классу опасности. Поставщиками ртути в атмосферу являются предприятия и заводы
, использующие её в своём производстве.
При попадании ртути в воздух, водоёмы и почву происходят процессы образования органических соединений, отличающихся высокой токсичностью.
Накопление в организме ртути и ртутных соединений приводит к поражению кожных покровов, дыхательных путей, внутренних органов, нервной и кроветворной систем.
Из природного компонента ртуть превратилась в угрозу для здоровья человека.
До 1937 г. добыча ртути в США не превышала обычно 700 т в год.
В зависимости от спроса добыча ртути и цена на нее меняются в значительных пределах. При нормальных условиях, когда не будет повышенного спроса на ртуть для военных целей, цена ртути на мировом рынке должна быть в пределах 0 75 - 1 долл кг.
В 1994 г. была прекращена добыча ртути.
В таблице приведены данные статистики добычи ртути в разных странах.
Встречается в природе в виде руды и служит для добычи ртути.
Использование ртути как рабочего вещества паросиловых установок ограничивается все же следующими обстоятельствами: разведанные запасы и добыча ртути относительно невелики, а стоимость ее сравнительно высока.
Однако хроническое прерывистое отравление, при котором периоды активной интоксикации перемежаются с периодами латентной интоксикации, до сих пор могут обнаруживаться среди работников предприятий по добыче ртути. В латентные периоды симптомы ослабляются до такой степени, что они заметны лишь при внимательном обследовании; сохраняются лишь неврологические проявления в форме обильного потоотделения, дермографизма и, в некоторой степени, эмоциональной нестабильности.
Отдельные группы шахтеров сталкиваются и с некоторыми другими вредными факторами - загрязнителями воздуха. Работающие на золотых приисках и в обогатительных цехах, а также на добыче ртути подвергаются воздействию ртутных паров и, следовательно, риску отравления ртутью. На золотых приисках и свинцовых рудниках имеет место воздействие мышьяка и риск заболевания раком легких. На никелевых рудниках воздействие никеля повышает риск заболевания раком легких и кожными аллергическими реакциями.
Даже тогда, когда причинно-следственная связь между воздействием препарата и последующим отравлением была установлена, наши предки часто придерживались политики приемлемого риска. В этом случае риск считался приемлемым, поскольку добычей ртути занимались заключенные и рабы.
Основным промышленным материалом является киноварь. Известно также уникальное месторождение Гуитцуко (Мексика), где главный рудный материал - ливингстонит. В некоторых случаях промышленные запасы ртути наблюдаются в месторождениях, главным минералом которых является амальгама серебра, например месторождение Нью-Альмаден (Мексика), где в течение ряда лет проводилась добыча ртути. Подавляющая часть ртути заключена в собственно ртутных месторождениях. Значительно меньшее промышленное значение имеют ртутно-сурьмяные, ртутно-мышьяковые и ртуть-еодержащие золотые и полиметаллические руды.
Основной рудой для добычи ртути является киноварь (HgS) - минерал яркокраеного цвета. По первому способу руды ртути или предварительно обогащенные концентраты подвергаются окислительному обжигу в специальных печах с одновременным восстановлением до металла. При этом ртуть, обладающая низкой температурой кипения (356 9), испаряется и конденсируется в специальных приемниках. Гидроме-таллургическкй способ добычи ртути применяется значительно реже и состоит из выщелачивания сернистым натрием сульфита ртути (HgS) из руд или содержащих ртуть хвостов, получаю - щихся при амальгамации серебряных руд и концентратов, и осаждения ртути действием на раствор металлического алюминия в присутствии щелочи.
Пласты эти, тянущиеся между Азовскою и Константиновскою дорог [ ами ] имеют падение на юго-запад, следовательно простирание с северо-запада на юго-восток, а отвечающие им пласты, выступающие севернее Азовской дороги, падают на северо-восток, имея почти то же простирание. Притом здесь же и конец подъема, именно как раз около места схождения упомянутых дорог, недалеко от Щерби-новки и мест, арендуемых г-ном Шейерманом. Далее к северо-востоку пластовый выход поворачивает и переходит в тот ряд пластов, который лежит севернее Азовской дороги. В промежуточной полосе угля нет, пласты его разорваны или срезаны природой, здесь выступили нижние породы, и здесь-то найдены долгими личными усилиями горного инженера г-на Миненкова те кварцевые пласты с киноварью, на которых гг. Ауэрбах, Половцев и К основали добычу ртути. Посетив завод, идущий под руководством г-на Ми-яенкова, видев остатки древних разносов, оставшихся на выходе тех же кварцевых пластов, я убедился лично, что здесь прочно оснуется русская добыча ртути, которой вообще на свете мало и которая весьма важна и особенно для извлечения золота и серебра. Южные выходы угольных пластов все усеяны шахтами, и поучительно видеть, как линии расположения шахт тянутся на десятки верст параллельно друг другу все в одном и том же направлении.
Страницы: 1
Ещё в 3-м тысячелетии до н.э. в лечебных целях, в качестве пигмента, косметического средства и для амальгамации золота . Следы древних разработок сохранились в ряде районов Азии, Европы , в т.ч. и на нынешней территории (Средняя ). Многие ртутные мира были открыты по следам древних работ. Во 2-й половине 19 века основными центрами ртутной промышленности были Испания , Италия и .
Сокращение производства ртути обусловлено необходимостью осуществления дорогостоящих природоохранных мероприятий, структурными сдвигами в потреблении, нерентабельностью производства. В связи со снижением цен на ртуть в 1975 создана международных ассоциация производителей ртути "ASSIMER". Повышается значение вторичной ртути.
Ртутная промышленность несоциалистических стран по объёму производства, стоимости выпускаемой продукции и числу компаний-продуцентов сравнительно мала. Почти вся добыча сосредоточена на нескольких месторождениях. Предприятия ртутной промышленности Испании, Алжира, Турции, Италии полностью или частично принадлежат государству. Производством ртути в США и Мексике владеет частный сектор. Ведущие компании по добыче руд и производству ртути: "Mines de Almaden" (Испания), "Placer AMAX" (США), "Sonarem" (), "Etibank" (). Техника и технология добычи, обогащения руд и производства ртути за рубежом незначительно отличается от принятых в CCCP. Добыча ведётся подземным и, в возрастающей степени, открытым способами.
Первое место в мировом производстве ртути принадлежит Испании, где добыча комбинированным способом осуществляется в основном на месторождении Альмаден и на соседнем, недавно открытом месторождении Энтредичо. Производственная мощность до 1 млн. т руды в год. Потребление ртути в стране незначительное, поэтому практически вся ртуть идёт на экспорт. В США добыча и производство ртути осуществляются на месторождении Мак-Дёрмитт в штате Невада. Мощность карьера 150-300 тысяч т руды в год. В Турции существуют небольшие предприятия по добыче руд — шахты "Халикёй", "Конья" и др. (их мощность 150-300 тысяч т руды в год). В число крупных поставщиков ртути на внешний рынок выдвинулся Алжир, где открытым способом разрабатывается группа месторождений в районе Аззаба (Mpa-Сма и др.).